目前国内创新药领域内充斥着各种“Me-too”类新药,引起了监管部门的关注,并拟出台政策对这样的现状进行引导。其实,“Me-too”是资本趋利避害的一种本性罢了,因为“First-in-Class”不仅难度太大,而且周期动则以十年计算,不利于资本快速变现的要求。但是,中国创新药真正的未来并不在这些“Me-too”、“Me-better”等处,而在于那些明知山有虎,偏向虎山行的“First-in-Class”身上。
华领医药就是“First-in-Class”的优秀代表之一。但是在其即将成功之际,似乎也有一丝隐忧。
有望First-in-Class,背后商业价值几何?
近日,在苏州举办的第六届中国医药创新与投资大会上,中华医学会糖尿病学分会常委、南京市第一医院内分泌科主任马建华教授作为主要研究者之一,公布了一项名为DREAM的临床研究结果,研究显示华领医药全球首创新药葡萄糖激酶激活剂Dorzagliatin有望在糖尿病缓解方面取得进展。
DREAM研究在中国5家研究中心、共69名患者中开展,研究结果显示,研究期内,受试者52周糖尿病缓解率为65.2%。这无疑是自今年4月Dorzagliatin新药上市申请获国家药监局受理后的又一重大研究进展。
Dorzagliatin是一种口服、小分子的GK(葡萄糖激酶)正向变构调节剂(GKA)。在健康成年人中,GK是一种酶,对葡萄糖具有适当的敏感性,因此血液中葡萄糖水平升高时,GK的活性相应升高。而在2型糖尿病患者中,GK的功能受损,即使在葡萄糖水平升高时,GK也保持不活跃状态。
作为一种完全活性、双重作用的GKA,Dorzagliatin可以根据患者的葡萄糖水平同时调节胰腺中的GK葡萄糖感应器功能及肝脏中的GK处理器功能。具体而言,Dorzagliatin包含独特的化学结构可以减少人体代谢物积累,通过调节GK的酶活性,改善2型糖尿病患者的已受损葡萄糖感应器功能。
在这条国际医药巨头纷纷入局的赛道上,截至目前,Dorzagliatin是全球范围内首个提交新药上市申请的葡萄糖激酶激动剂类(GKA)糖尿病治疗药物,预计于2022年第一季度获批上市,有望成为在中国首先上市的全球首创新药(First-in-Class)。
因此,华领医药正在紧锣密鼓地布置Dorzagliatin获批上市后的商业化进程。
2020年8月,华领医药与全球医药巨头拜耳就Dorzagliatin在中国的商业化达成战略合作协议,华领医药获得3亿元预付款,以及41.8亿元的销售里程碑付款。拜耳获得该产品在中国独家商业化的权利;
2020年9月,获得由上海市药监局颁发的Dorzagliatin《药品生产许可证》,完成商业化生产准备的核心工作;
2020年12月,与九洲药业旗下瑞博制药达成商业化生产供应协议;
2021年9月,华领医药与国药控股签署供应链战略合作协议。
此外,华领医药还在上海临港新片区设立生产基地,以确保Dorzagliatin充足的商业供应。无论是临床试验推进、商业化合作竞争及产能储备这一切的一切都在为Dorzagliatin规模话上市做足了准备。一直以来Dorzagliatin从进入临床试验阶段起就备受关注,那么如果顺利获批上市,是否会在降糖药市场中占据优势地位啦?
广袤却复杂的竞争格局,实不乐观
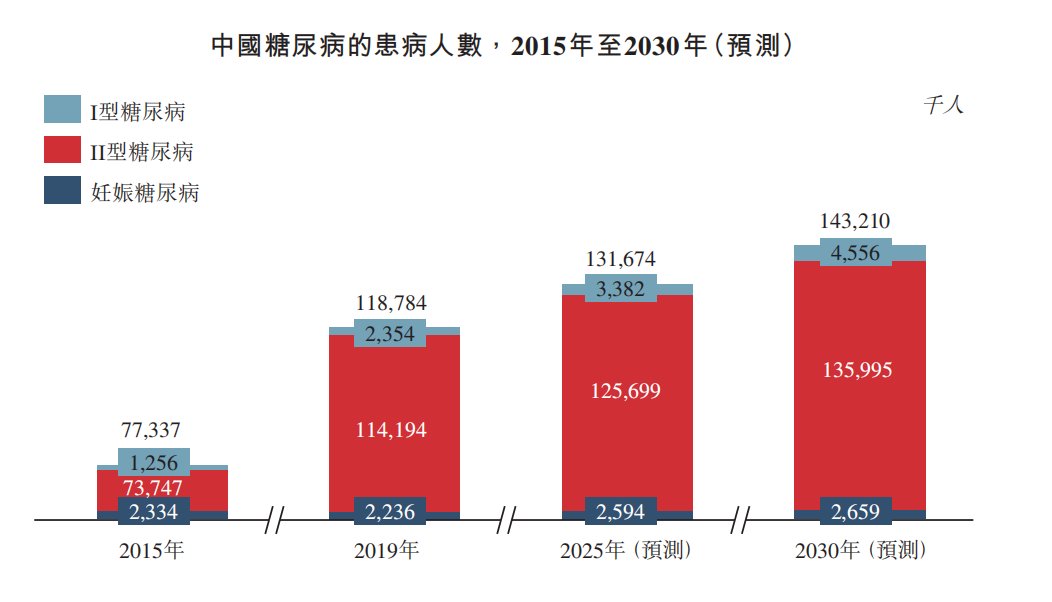
从疾病类型上来说,糖尿病主要有四种,即I型糖尿病、II型糖尿病、妊娠糖尿病、特殊类型糖尿病。其中II型糖尿病占所有糖尿病病例90%左右,常见于成年人,患病时,身体无法有效利用自身所产生的胰岛素。也是全球糖尿病领域主要关注的研究方向。
目前,全球范围内的糖尿病患病人数正在不断增加,其很大程度上归因于II型糖尿病的激增及包括人口老龄化、肥胖程度增加、饮食不健康、普遍身体活动不足等在内的相关因素。
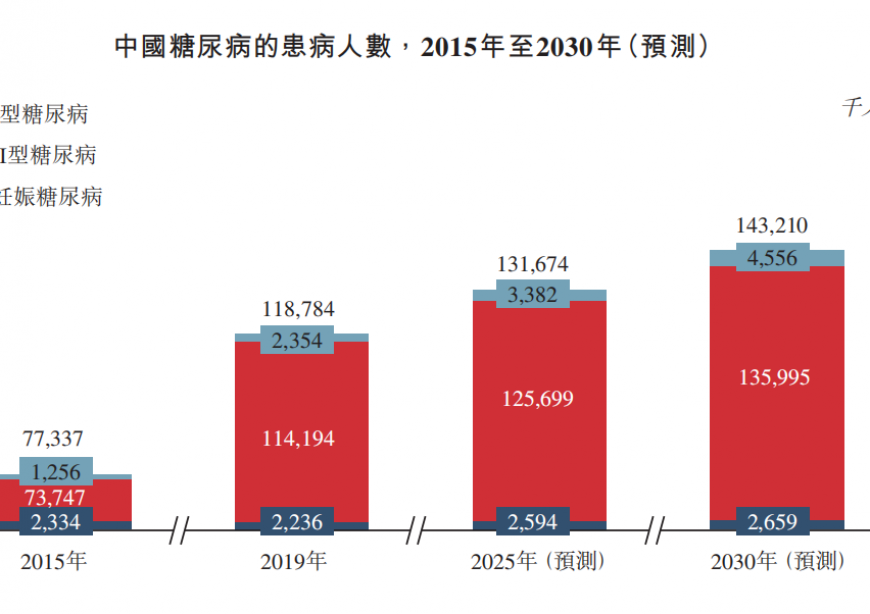
据统计,中国是世界上糖尿病患者最多的国家,II型糖尿病患者的数量在2019年就达到了1.14亿例,预计于2030年将增至1.36亿例,年复合增长率为1.6%。糖尿病几乎可影响人体的每个部位,因此必须有效管理糖尿病,每年治疗糖尿病的花费成百上千亿元。
同时,在治疗上目前中国并无清晰的治疗II型糖尿病的一线方案,各种防治指南也没有统一的口径。市面上共有九大类降糖药,其中七款为口服药,两款为注射液。口服药主要有盐酸二甲双胍、磺脲类药物、格列奈类药物、TZDs类药物、α-糖苷酶抑制剂、DPP-4i、SGLT2i;注射用药有GLP-1受体激动剂和胰岛素及其类似物。
而在各大类降糖药中,又各自存在数种主要产品,如α⁃糖苷酶抑制剂主要产品有阿卡波糖、伏格列波糖和米格列醇;磺脲类药物,国内上市的主要为格列本脲、格列美脲、格列齐特、格列吡嗪和格列喹酮;格列奈类药物,主要有瑞格列奈、那格列奈和米格列奈;DPP⁃4i,主要为西格列汀、沙格列汀、维格列汀、利格列汀和阿格列汀;SGLT2i,主要有达格列净、恩格列净、卡格列净和艾托格列净;TZDs类药物,主要有罗格列酮和吡格列酮及其与二甲双胍的复方制剂;胰岛素也有二代、三代、速效、长效之分;GLP-1受体激动剂代表药物有艾塞那肽、利拉鲁肽等。
近年来,一些用量大的降糖药遭遇了集采的重大打击。第二批国家集采中,拜耳的原研阿卡波糖单片报出了0.18元,以超低价中标;第三批国采中,盐酸二甲双胍0.5g规格的单片平均价仅为6分钱;第四批集采纳入的糖尿病治疗药物有恩格列净、卡格列净、格列齐特、那格列奈和瑞格列奈;而胰岛素集采马上就要在十月份打响,预计又是一片血雨腥风。
在这样一个看似市场广阔、实则治疗药物拥挤,治疗方案众多的赛道里,Dorzagliatin作为一款First-in-Class的药物除了展现创新能力,鼓舞行业同仁外,更受关注的实际意义又有多少?
成也“Dorzagliatin”,败也会是“Dorzagliatin”吗?
在可以预见的未来,Dorzagliatin获批上市是大概率事件。但是从某种意义上来讲,Dorzagliatin的成功并不意味着华领医药就一定会成功。
作为一家尚未有任何产品上市销售的创新药公司,华领医药自2018年上市以来,三年间净利润经调整后的亏损分别为2.79亿元、3.51亿元、3.94亿元;研发支出分别为2.69亿元、3.22亿元、2.21亿元。2021年上半年亏损1.65亿元、研发支出0.98亿元。
或许说,如此亏损和研发支出在这两年新上市的众多创新药企业中并不算夸张,但华领医药最大的问题在于其研发管线过于单一。目前华领医药的研发管线中,共有9个在研项目,除了Dorzagliatin单药研发之外,还有6个项目是Dorzagliatin与其他降糖药的联合用药临床试验,分别是Dorzagliatin+二甲双胍、Dorzagliatin+西格列汀、Dorzagliatin+恩格列净、Dorzagliatin+吡格列酮、Dorzagliatin+GLP-1、Dorzagliatin+胰岛素,这6项联合用药项目基本都还处于临床试验早期阶段,离成功还有很长一段距离。
另外两个项目中用于治疗帕金森症左旋多巴诱发的异动症不自主运动(PD-LID)的mGLUR5NAM和用于治疗代谢性疾病的果糖激酶抑制剂,且两者均还处于临床前阶段。也就是说,华领医药的弹药库里基本全是与Dorzagliatin相关的项目。
也正是华领医药“单品独大”这一特点,在资本市场却是避之不及的一条投资法则。因此,华领医药的股价才会从发行价每股9.28港元,一路下滑。即使目前Dorzagliatin已提交上市申请,却仍难有上扬趋势,目前总市值约48亿港元。
要知道,华领医药在2009年就已经成立,目前国内创新药企领头羊百济神州还比之晚一年成立。并且,其2011年就已经从罗氏引进开发Dorzagliatin,至今已整整十年,这让作为创新药“前辈”的华领医药情何以堪啦!
当然,创新药领域单品独大,却仍能斩获成功的案例也不是没有,贝达药业凭借一款埃克替尼挣了十年。但今时不同往日,集采将行业格局全部打乱,创新药企如雨后春笋般涌现,布局慢性病用药的企业越来越多,且未来竞争还会更加激烈。要想在这样的环境中生存下去,各大创新药企都在努力地打造差异化研发管线,普遍规律下反而是管线层次越分明,品种越丰富,越受资本市场追捧,如百济、信达等。
这无疑与华领医药选择之道路背道而驰,以目前情况看来,大势已定。如若华领医药能依靠账上8.45亿元的现金流与未来即将变现的Dorzagliatin收益,尝试License-in,也许还有突破的希望。
结语
当然,一味强调管线丰富、差异化的企业才有前途却也是一个有失偏驳的行为,谁说“小而美”就不能是企业发展路径,医药行业这一条广袤产业链也不是几家大型药企就能撑起来的,其中每个环节、每个阶段都值得被尊敬。
未来,只希望华领医药能用其坚韧的研发精神为中国带来更多的“First-in-Class”新药,为中国真正的创新多多贡献自己的力量。相信未来随着Dorzagliatin的成功商业化,华领医药将有更多的精力和实力带来惊喜。后续发展如何,还将持续关注。